目次
クリングルファーマの概要
クリングルファーマの基本情報
はじめに、クリングルファーマ株式会社の基本情報を紹介します。
上場予定日は2020年12月28日、市場はマザーズ、想定時価総額は40.2億円です。
| 会社名 | クリングルファーマ株式会社 |
|---|---|
| 設立日 | 2001年12月21日 |
| 上場日 | 2020年12月28日(承認日:2020年11月24日) |
| 市場 | マザーズ |
| 証券コード | 4884 |
| 業種 | 医薬品 |
| 決算期 | 12月 |
| ホームページアドレス | https://www.kringle-pharma.com/ |
| 発行済株式総数 | 3,647,700 株(2020 年 11 月 24 日現在) |
| 上場時発行済株式総数 | 4,227,700 株 ※公募分を含む。 ※新株予約権の権利行使により増加する可能性がある。 |
| 公募株数 | 580,000 株 |
| 想定価格 | 950 円 |
| 想定時価総額 | 40.2 億円(※上場時発行済株式総数×想定価格で計算) |
| 資本金 | 300,000 千円(2020 年 11 月 24 日現在) |
| 1単元の株式数 | 100 株 |
| 監査人 | EY 新日本有限責任監査法人 |
| 主幹事証券会社 | 野村證券 |
| 引受幹事証券会社 | SBI証券 SMBC日興証券 楽天証券 三菱UFJモルガン・スタンレー証券 いちよし証券 東洋証券 エース証券 岡三証券 |
クリングルファーマの沿革
クリングルファーマは、2001年に大阪府において設立され、医薬品・遺伝子治療に関する研究開発を目的として設立されました。
その後、大阪大学などと提携を組み、現在では難治性疾患の治療薬の研究開発に注力しています。
| 2001年12月 | 医薬品、遺伝子治療に関する研究開発を事業目的として、大阪市北区にクリングルファーマ株式会社(資本金10,000千円)を設立 |
| 2002年8月 | 本社を大阪市北区から大阪市中央区に移転 |
| 2004年7月 | 本社を大阪市中央区から大阪府豊中市に移転 |
| 2004年10月 | 大阪府茨木市に研究所を開設 |
| 2005年5月 | 中村敏一氏(当時:大阪大学大学院医学系研究科教授)より、HGF(Hepatocyte Growth Factor: 肝細胞増殖因子)タンパク質の開発実施権の許諾を得て、新規パイプラインとして開発を開始 (開発コード:KP-100) |
| 2007年6月 | GMP準拠によるKP-100原薬(HGFタンパク質を主成分とする原薬)を量産する製造方法を確立 |
| 2007年7月 | HGFに関する基礎研究を目的として国立大学法人大阪大学にクリングルファーマ再生創薬研究部門を開設(2012年3月に閉鎖) |
| 2007年11月 | HGFからなる動物用医薬品の早期実用化を目的として、日本全薬工業株式会社と共同研究契約及びライセンス契約を締結 |
| 2008年10月 | ノルウェーにおいて、KP-100を主成分とする製剤(ChronSeal®)について、皮膚潰瘍患者を対象と した第Ⅰ/Ⅱ相試験を開始 |
| 2008年12月 | 米国において、慢性腎不全患者を対象とするKP-100の第Ⅰa相試験を開始 |
| 2009年1月 | 皮膚領域の臨床開発の円滑な推進を目的として、スウェーデンにKringle Pharma Europe AB(連 結子会社)を設立(2011年3月に清算) |
| 2009年7月 | スウェーデンにおいて、皮膚潰瘍患者を対象としたChronSeal®の第Ⅰ/Ⅱ相試験を開始 |
| 2010年8月 | 米国における、慢性腎不全患者を対象とするKP-100の第Ⅰa相試験を終了 |
| 2010年9月 | ノルウェー及びスウェーデンにおける、皮膚潰瘍患者を対象としたChronSeal®の第Ⅰ/Ⅱ相試験 を終了 |
| 2011年12月 | 米国において、慢性腎不全患者を対象とするKP-100の第Ⅰb相試験を開始 |
| 2012年4月 | 日本において、筋萎縮性側索硬化症(以下、「ALS」という)患者を対象としたKP-100ITの第Ⅰ相 試験を開始 |
| 2012年6月 | 米国における、慢性腎不全患者を対象とするKP-100の第Ⅰb相試験を終了 |
| 2014年6月 | 本社を大阪府豊中市から大阪府茨木市に移転 日本において、脊髄損傷急性期患者を対象としたKP-100ITの第Ⅰ/Ⅱ相試験を開始 |
| 2014年11月 | 日本において、声帯瘢痕患者を対象としたKP-100LIの第Ⅰ/Ⅱ相試験(医師主導)を開始 |
| 2015年3月 | 日本における、ALS患者を対象としたKP-100ITの第Ⅰ相試験を終了 |
| 2016年5月 | 日本において、ALS患者を対象としたKP-100ITの第Ⅱ相試験(医師主導)を開始 |
| 2016年11月 | 日本における、声帯瘢痕患者を対象としたKP-100LIの第Ⅰ/Ⅱ相試験(医師主導)を終了 |
| 2018年6月 | クリングルファーマが製造した組換えヒトHGFタンパク質を株式会社リプロセルより研究用試薬として販売開始 |
| 2018年10月 | 日本における、脊髄損傷急性期患者を対象としたKP-100ITの第Ⅰ/Ⅱ相試験を終了 |
| 2019年9月 | 厚生労働省が脊髄損傷急性期を対象とするKP-100ITを希少疾病用医薬品として指定 |
| 2020年3月 | 東邦ホールディングス株式会社との資本業務提携を通じて、脊髄損傷急性期を対象とする KP-100IT医薬品の卸売流通体制を構築 |
| 2020年4月 | 米国クラリス・バイオセラピューティクス社とライセンス及びKP-100原薬の供給契約を締結 |
| 2020年7月 | 日本において、脊髄損傷急性期患者を対象としたKP-100ITの第Ⅲ相試験を開始 |
| 2020年8月 | 丸石製薬株式会社との資本業務提携を通じて、脊髄損傷急性期を対象とするKP-100IT医薬品の販 売体制を構築 |
クリングルファーマの事業内容
クリングルファーマは、「難治性疾患治療薬の研究開発を行い、難病に苦しむ患者さんに対して画期的な治療手段を提供し、社会に貢献いたします」を経営理念として掲げ、症例が少なく治療法が確立していない疾患に対する製薬の研究開発を目的とした事業を運営する企業です。
以下は、クリングルファーマの事業モデルを表した図になります。
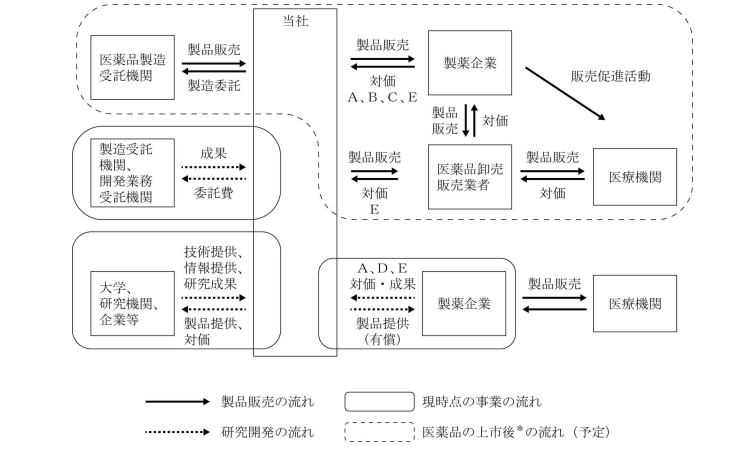
① 事業の概要
クリングルファーマは、「症例数が少なく、原因不明で、治療法が確立しておらず、生活面への長期にわたる支障がある疾患」(難治性疾患)に対する治療薬の研究開発を目指す大学発バイオベンチャーとして設立されました。
クリングルファーマが臨床試験段階まで到達している難治性疾患の対象は、現在「脊髄損傷急性期」「急性腎障害」「ALS(筋萎縮性硬化症)」「声帯瘢痕」とされています。
クリングルファーマでは、このような難治性疾患疾患を治療するため、中村敏一氏(当時:大阪大学大学院医学系研究科教授)の発見したHGF(肝細胞増殖因子)タンパク質を医薬品になる可能性のある候補物質として導入し、研究開発や臨床試験を複数回実施してきました。
また、従来の創薬バイオベンチャーは、臨床試験まで研究成果を製薬企業に提出しその後の開発・製造販売を委ねるのが一般的ですが、クリングルファーマでは、医薬品の製造販売承認を得る段階まで自社で開発を進める方針で事業を推進しています。
なお、クリングルファーマの研究領域である主要な製品と研究段階(2020年10月時点)は以下の図の通りです。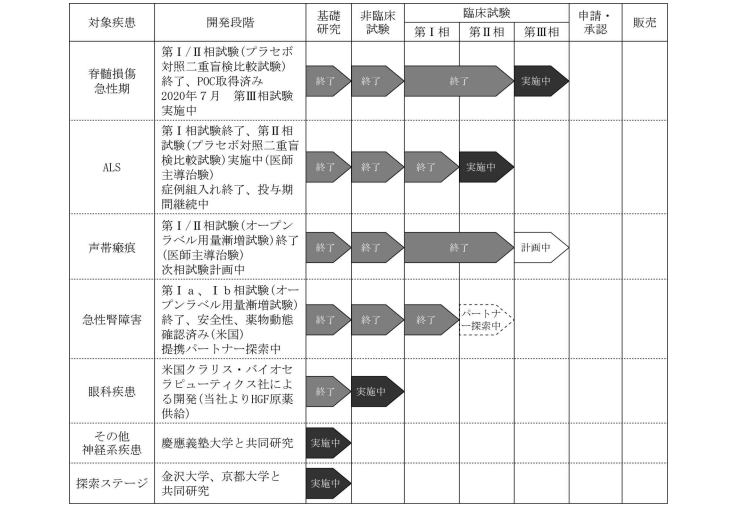
② ビジネスモデル
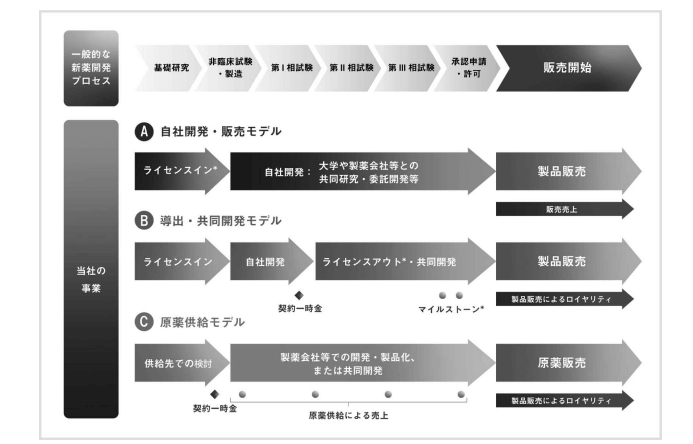
クリングルファーマでは、以下の3つのビジネスモデルで収益化が行われています。
- 自社開発・販売モデル
自社や他社と共同で製品販売までのプロセスを全てに完結させるビジネスモデル。 - 導出・共同開発モデル
販売に至る途中段階まで自社で製品を開発し、その後ライセンスを譲渡し、譲渡したライセンスに応じた収益を計上するモデル。 - 原薬供給モデル
原薬供給までの役割を担い、原薬供給に応じた収益を獲得するモデル。
クリングルファーマは、上記の3つのモデルを対象疾患や提携先に応じて組み合わせたハイブリッド型の事業モデルを採用しています。
なお、各モデルをビジュアル化した図は以下の通りです。
有価証券報告書情報
経営指標(過去2期分)
第18期の業績は以下の通りです。
- 売上高:-億円
- 経常利益:△3.0億円
- 当期純利益:△3.0億円
| 期 | 第17期 | 第18期 |
| 決算年月 | 2018年9月 | 2019年9月 |
| 売上高(千円) | – | – |
| 経常利益(千円) | △64,134 | △301,630 |
| 当期純利益(千円) | △64,554 | △302,050 |
| 純資産額(千円) | 518,443 | 216,393 |
| 総資産額(千円) | 566,928 | 251,868 |
| 自己資本比率 | 91.4% | 85.9% |
| 営業キャッシュフロー(千円) | △202,416 | △338,801 |
| 投資キャッシュフロー(千円) | 1 | – |
| 財務キャッシュフロー(千円) | 199,274 | – |
| 現金・現金同等物の期末残高(千円) | 505,278 | 166,476 |
| 従業員数 | 5人 | 6人 |
経営指標(過去5期分)
過去5期の業績を見ると、売上高は計上されておらず、赤字の状態が続いていることがわかります。
また、第14,15期は、債務超過の状態に陥りましたが、16期以降は債務超過からは脱しています。
売上が計上されていない原因は、クリングルファーマが開発している医薬品は、研究段階もしくは臨床試験段階であり、まだ市場での販売が行われていないため、収益が計上されていないからです。
また、医薬品の開発は、一般的に莫大な研究開発費用や時間を費やすため、製品が実際に市場に出て収益化されるまでに時間がかかることが特徴の一つです。
| 期 | 第14期 | 第15期 | 第16期 | 第17期 | 第18期 |
| 決算年月 | 2016年2月 | 2016年9月 | 2017年9月 | 2018年9月 | 2019年9月 |
| 売上高(千円) | – | – | – | – | – |
| 経常利益(千円) | △197,813 | 101,696 | △101,676 | △64,134 | △301,630 |
| 当期純利益(千円) | △200,337 | 100,206 | △102,096 | △64,554 | △302,050 |
| 資本金(千円) | 100,000 | 100,000 | 100,000 | 100,000 | 100,000 |
| 発行済株式総数 | 52,053 | 52,053 | 113,053 | 121,053 | 121,053 |
| 純資産額(千円) | △225,112 | △124,905 | 382,997 | 518,443 | 216,393 |
| 総資産額(千円) | 237,558 | 107,321 | 532,750 | 566,928 | 251,868 |
| 自己資本比率 | △94.8% | △116.4% | 71.9% | 91.4% | 85.9% |
| 従業員数 | 2人 | 2人 | 5人 | 5人 | 6人 |
クリングルファーマ株式会社は2020年3月、複数の企業やファンドを引き受け先とした第三者割当増資を実施し、9億5千万円を調達したことを発表しました。
この増資による調達資金は、主に脊髄損傷急性期を対象とする第Ⅲ相試験の準備と実施、製造販売承認申請を見据えたHGFタンパク質のGMP製造資金に充当され、HGFタンパク質性医薬品の開発を加速させる意向であるとしています。
さらにクリングルファーマは、2020年4月に複数のファンドや個人投資家を引受先とした第三者割当増資によって、7億4千万円を追加調達を実施しています。
また、調達資金の目的は上述したHGFタンパク質性医薬品の開発に充当するとされています。
クリングルファーマ株式会社は9億5千万円の第三者割当増資を実施しました
クリングルファーマ株式会社は第三者割当増資により7億4千万円を追加調達しました
株主構成
上位10位までの主要な株主は、以下の通りです。
| 株主 | 所有株式数 | 比率 | ロックアップ |
| 日本全薬工業株式会社 | 500,840 | 12.12% | 90日間 |
| 慶應イノベーション・イニシアティブ1号投資事業有限責任組合 | 470,460 | 11.38% | 90日間 |
| DBJキャピタル投資事業有限責任組合 | 319,800 | 7.74% | 90日間 |
| THVP-1号投資事業有限責任組合 | 226,660 | 5.48% | 90日間 |
| CYBERDYNE株式会社 | 200,000 | 4.84% | 90日間 |
| OUVC1号投資事業有限責任組合 | 200,000 | 4.84% | 継続保有 |
| 安達 喜一 | 171,900 | 4.16% | 90日間 |
| 岩谷 邦夫 | 132,040 | 3.20% | 90日間 |
| 丸石製薬株式会社 | 100,000 | 2.42% | 継続保有 |
| 株式会社リプロセル | 100,000 | 2.42% | 90日間 |
新規上場(IPO)の募集・売出し情報
公募・売出し・調達額情報
想定価格は950円、吸収金額(調達額)は 6.3億円と予想されています。
| 仮条件 | 未発表 |
|---|---|
| 公募・売出価格 | 未発表 |
| 想定価格 | 950 円 |
| 初値 | – |
| 公募株数 | 580,000 株 |
| 売出株数 | – |
| オーバーアロットメントによる売出し株数 | 87,000 株 |
| 吸収金額(調達額) | 6.3 億円 (※オーバーアロットメントを含む株数×想定価格で計算) |

 赤堀 太紀 FAST法律事務所 代表弁護士
企業法務をはじめ、債務整理関連の案件、離婚・男女トラブルの案件、芸能関係の案件などを多数手がける。
赤堀 太紀 FAST法律事務所 代表弁護士
企業法務をはじめ、債務整理関連の案件、離婚・男女トラブルの案件、芸能関係の案件などを多数手がける。













